A PCOS betegeknél, akiknél meddőségi panasz is van, a terápiás lehetőségeket három fő csoportba osztjuk. A hagyományos eljárások mellett, új lehetőséget jelent az inzulinrezisztencia csökkentésére ható készítmények. Mindig a legegyszerübb eljárással kezdjük a betegek kezelését. A tájékoztató randomizált kontrollált vizsgálatok (RTC), meta-analysisek és a Cochrane adatbázisban szereplő adatok alapján foglalja össze a terápiás lehetőségeket. (G.S.)
TARTALOM
Kutatási típusok és rövidítések értelmezése
1. A kezelés első lépcsője (Clomifen-citrát)
2. A kezelés második lépcsője (gonadotropinok, műtéti eljárások)
3. A kezelés harmadik lépcsője: IVF
4. Metformin alkalmazása meddőség esetén
5. Inositol alkalmazásának lehetősége
6. Szelektív aromatáz inhibitorok alkalmazásának lehetősége
Kutatási típusok és rövidítések értelmezése
CI: (confidence interval) megbízhatósági tartomány, konfidencia intervallum. A becslések bizonytalanságának számszerűsítésekor az az intervallum, amely egy bizonyos (szokásosan 95%-os vagy 99%-os) valószínűséggel magában foglalja a becsült populációs paraméter valódi értékét. Határai kiszámíthatók a becslés hibájából vagy egzakt valószínűségszámítási módszerekkel.
Cochrane szisztematikus irodalmi értékelés: A szisztematikus összefoglalók Cochrane adatbázisában fellehető rendszerezett irodalmi áttekintések, melyek az egyes gyógyító-megelőző eljárások klinikai hatásosságát és nem kívánt mellékhatását tekintik át. Ezek a hétköznapi rutin gyógyító ellátás során felmerülő klinikai kérdésekre próbálnak praktikus választ adni, és egységes, szigorú módszertan szerint készülnek.
meta-analízis: Több hasonló célú vizsgálat eredményeiből készült összesített, átfogó elemzés. Legfőbb előnye, hogy minden elérhető adattal számol, így nagyobb statisztikai erővel bír, mint az egyes vizsgálatok külön-külön, ezért egy-egy metaanalízis megbízhatósága igen jelentős.
ICSI: Intracitoplazmatikus Spermium Injektálás az IVF (lombikbébi) kezelés egyik válfaja.
IVF-ET: in vitro fertilisatio (IVF) és embryo transfer (ET).
OR (odds ratio) esélyhányados, EH: Kutatások során számolt kapcsolati mutató. Az esélyhányados két összehasonlítandó (pl. kezelt vagy nem kezelt) csoport eredményének a hányadosa. Tehát annak az esélyét mutatja, hogy a kezelésnek milyen a várható eredménye a kontroll (kezelésben nem részesült vagy egy alternatív kezelésben részesülő) csoporthoz viszonyítva.
RTC: (randomized controlled trial) randomizált kontrollált tanulmány: A résztvevőket két csoportra osztják, az egyik csoportot kiteszik valamilyen beavatkozásnak, míg a másik csoportban nem végzik el az adott beavatkozást. Ezt követően egy meghatározott idő elteltével vizsgálják a beavatkozás következményeként kialakuló valamilyen kimenetelt. A randomizált, kontrollált vizsgálat mindig prospektív vizsgálat, hiszen a vizsgálat tervezése megelőzte a megfigyelni kívánt eseményeket.
szisztematikus irodalmi áttekintés: Rendszerezett irodalmi összefoglaló, mely előre meghatározott, igényes tudományos módszertannal dolgozza fel az összes elérhető szakirodalmat, hogy elkerülje az irodalmi áttekintések leggyakoribb hibáit (pl. a publikációs hibából adódó közlési elfogultságot). A módszeres irodalmazást követően a tudományos közleményeket előre meghatározott feltételek alapján minőségi elemzésnek vetik alá, és a megfelelő vizsgálatok eredményeit kvalitatív vagy kvantitatív (metaanalízis) módszerrel összesítik. Ilyen rendszerezett irodalmi áttekintések találhatók a Cochrane Könyvtárban is.

Depositphotos_55162693_m-2015.jpg
NEM SZABAD ELFELEJTKEZNI ARRÓL, HOGY ELHÍZOTT PCOS BETEGEKNÉL - BÁRMELYIK KEZELÉS MELLETT - AZ ÉLETMÓDVÁLTOZTATÁS, A FOGYÁS NÉLKÜLÖZHETETLEN!
KÜLÖN IS FELHÍVOM A FIGYELMET, HOGY - BÁR A METFORMIN NÖVELI / NÖVELHETI A PETEÉRÉSEK ARÁNYÁT - ALKALMAZÁSA A MEDDŐSÉG KEZELÉSÉRE ÖNMAGÁBAN GYAKRAN NEM ELEGENDŐ!
1. A kezelés első lépcsője (Clomifen-citrát)
Túlsúlyos vagy elhízott PCOS betegeknél, még a gyógyszeres kezelés előtt, a testtömeg csökkentése javasolt. (életmód, Saxenda, Mounjaro)
Anovulációval járó infertilitás gyógyszeres kezelésének továbbra is első vonalbeli szere a clomifen-citrát (CC), a második vonalbeli kezelés a gonadotropinok alkalmazása. A CC kezdő adagja 25–50 mg/ nap a ciklus 2–5. napján. A dózis napi 150 mg-ig emelhető. A kezelés általában maximum hat cikluson keresztül folytatható. Amennyiben ezt követően sem esik teherbe a beteg és IR igazolható, kiegészítő metformin kiegészítő kezelés kísérlendő meg. A clomifen-citrát alkalmazásával a ciklusok 70–85%-ban lehet ovulációt igazolni, kummulatív terhességi ráta a hat havi kezelési időszakra vonatkozóan 50–60% közötti.
A clomifen-citrát (Clostilbegyt) hatását nem elegendő ultrahanggal ellenőrizni, a ciklus 21-23. napján progeszteron, ösztradiol, prolaktin vizsgálata is szükséges, továbbá - a klinikai helyzettől függően - a hím nemi hormonok (tesztoszteron, androsztendion, DHEAS) ellenőrzése is fontos információt jelent a készítmény eredményességéről vagy hatástalanságáról.
Ha a kezelés eredménytelen:
- Emelkedett DHEAS esetén, a ciklus 5–14. napja között, napi 2 mg kiegészítő dexamethason kezelés javítja az ovuláció indukció eredményességét.
- Emelkedett androsztendion estén metformin vagy inositol kezelés javítja a peteérés valószínűségét.
Megjegyzés: Tartós vérzéskimaradás esetén, csak gesztagenekkel (pl. Norcolut, Provera, Utrogestan) történő megvonásos vérzés után alkalmazott CC kezelés nem mindig eredményes, ugyanis a clomifen-citrat hatásához megfelelő szintű ösztrogénre is szükség van. Ilyenkor ösztrogén, majd ösztrogén + gesztagen kombinált terápiára van szükség, mielőtt a kezelés második lépcsője kerül alkalmazásra.
A clomifen-citrát kezelés eredményét a szöveti oxidatív stressz is befolyásolja. Utóbbi időben kimutatták, hogy a PCOS-ben szenvedő, ovulációs zavarokat tapasztaló nők csaknem 30%-a ellenáll a clomifen-citráttal végzett stimulációnak, amely az FSH hatására indukálja a tüszők növekedését. Ezeknél a betegeknél pozitív korrelációt találtak a pro-inflammatorikus CXCL16 kemokin és a CRP gyulladásos fehérje szérumszintje között. A CXCL-16 ronthatja a petefészek klomifen-citrátra adott válaszát az angiogenezis és a gyulladás fokozása révén, így blokkolja az ovulációt és a terhesség kialakulásához kapcsolatos problémákhoz vezethet.
2. A kezelés második lépcsője (gonadotropinok, műtéti eljárások)
2.1. Gonadotropinok alkalmazása
A kezelés második lépcsőjét a gonadotropinok jelentik. Tekintettel arra, hogy a petefészek FSH érzékenysége PCOS-ben megnő, a hiperstimuláció megelőzése érdekében alacsony, napi 37,5–50 IU kezdő dózis javasolt. Az FSH készítményt a ciklus 7–14. napja között javasolt alkalmazni, mindaddig, amíg ultrahanggal érett tüsző nem igazolható. A kezelés hatását E2 mérésekkel és follikulometriával szükséges ellenőrizni és ezek eredményei alapján adandó a humán koriogonadotropin (hCG) tartalmú készítmény az ovuláció kiváltására Az eddigi eredmények alapján a rekombináns FSH készítmények (follitropin alfa, follitropin beta) alkalmazása előnyösebb az urofollitropint tartalmazó készítményeknél.
A kis dózisú „step-up” FSH protokoll három ciklus alatt eredményesebb a CC kezelésnél. A terhességi arány 52,1% versus 41,2% (p = 0,021), kummulativ élveszületési arány 47,4% versus 36,9%, p = 0,031. Ugyanakkor a gonadotropin kezelés drágább a hagyományos CC kezelésnél, nagyobb az ovarialis hyperstimulatiós-szindróma (OHSS) kockázata, illetve a hCG-t vagy rekombináns LH-t tartalmazó készítmény alkalmazási időpontjának pontos meghatározása miatt nagyobb felügyeletet is igényel.
2.2. Műtéti eljárások alkalmazása
A műtéti eljárások ugyancsak a meddő PCOS beteg kezelésének második lépcsőjébe sorolhatók. Ezek közül a laparoscopias eljárással végzett petefészek-drilling (LOD) a legelterjedtebben ajánlott módszer. A műtéti beavatkozás előtt azonban különösen mérlegelni szükséges a várható előnyöket és kockázatokat, illetve azt, hogy már minden egyéb gyógyszeres terápiás lehetőséget kihasználtunk-e?

(kép: depositphotos.com)
A műtéti megoldás mérlegelésének szükségességét egy 2007-ben végzett Cochrane tanulmány eredménye támasztja alá.
Ez alapján az élveszületések számában nem volt különbség a LOD és az egyéb kezelések között: CC (OR: 1,21 [95% CI: 0,64–2,32]), gonadotropinok (OR: 0,97 [95% CI: 0,59–1,59], aromatáz gátlók (OR: 0,84 [95% CI: 0,54–1,31]). LOD elvégzése után szignifikánsan kevesebb volt az élveszületések száma is, a CC + MET kombinációval összehasonlítva (OR: 0,44 [95% CI: 0,24–0,82], p = 0,01).
3. A kezelés harmadik lépcsője: IVF
Meddő PCOS-s betegek kezelésének harmadik lépcsője az in vitro fertilizáció (IVF).
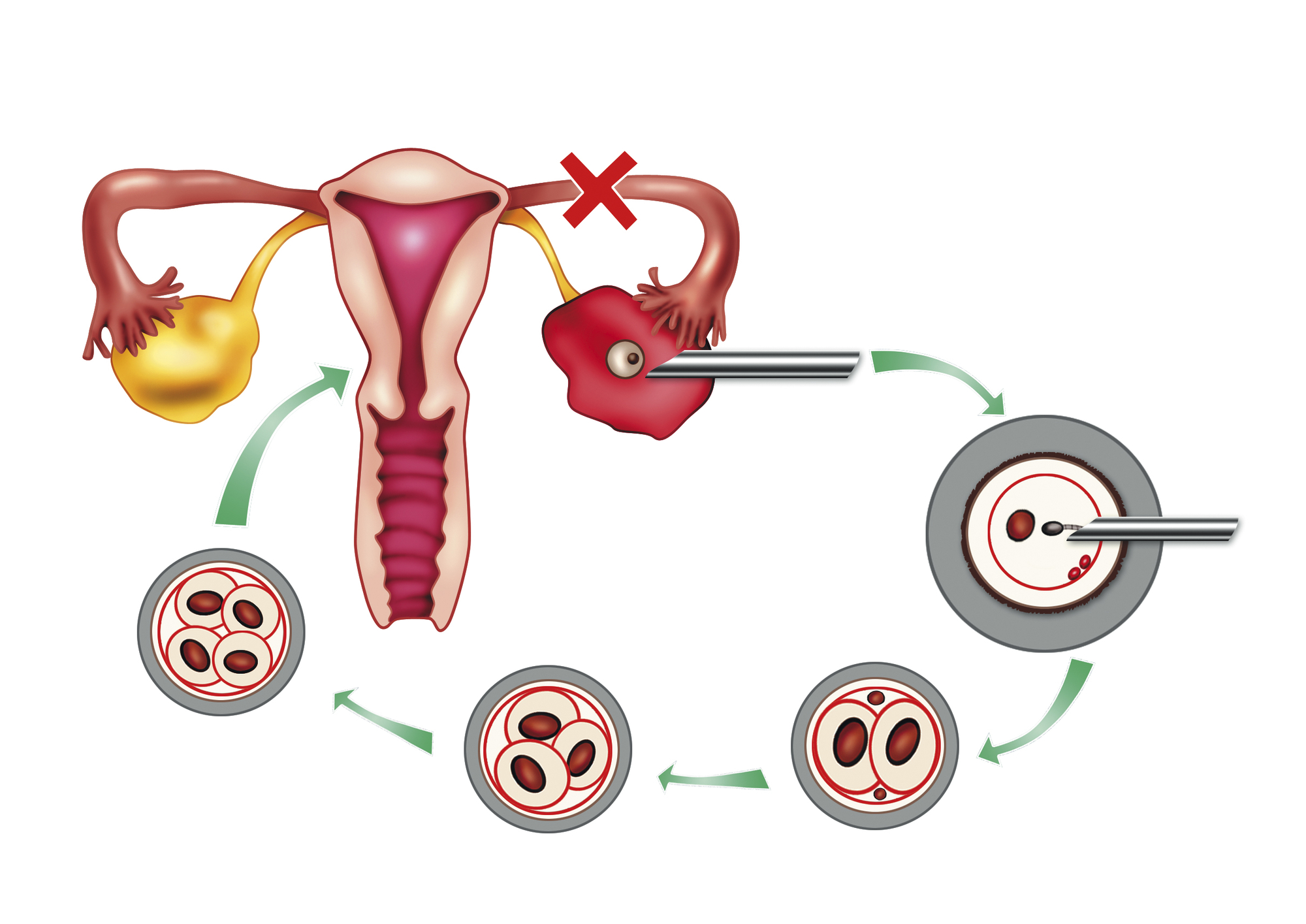 (kép: depositphotos.com)
(kép: depositphotos.com)
Meta-analízissel nem igazoltak különbséget "hosszú protokoll" szerint alkalmazott gonadotropin-releasing hormon (GnRH) agonisták (Ago) és GnRH antagonisták (Ant) között. Ugyanakkor valószínű, hogy a GnRH antagonisták csökkentik az OHSS kialakulását (OR: 0,36 [95% CI: 0,25–0,52]), a GnRH agonistákhoz viszonyítva. Ugyanakkor sem az oocyták, sem a klinikai terhességek számában vagy a vetélések arányában nem igazolható különbség.
4. Metformin alkalmazása meddőség esetén
A metformin alkalmazásának eredményessége meddőség kezelésére sem egyértelmű még. A NIH szerinti kritériumok alapján diagnosztizált PCOS tanulmányok szisztematikus értékelése szerint a MET a placebohoz viszonyítva szignifikánsan (P < 0,05) növeli a terhességek esélyét.
A nem elhízott PCOS betegeknél a MET és a CC hasonló arányban eredményez ovulációt (OR: 0,87 [95% CI: 0,60–1,26]). Elhízottaknál a CC kedvezőbb (OR: 0,43 [95% CI: 0,36–0,51]). Nem elhízott betegeknél a MET kedvezőbb a klinikailag igazolt terhesség szempontjából (OR: 1,94 [95% CI: 1,19–3,16]), míg elhízott betegeknél kedvezőtlenebb eredményességű (OR: 0,34 [95% CI: 0,21–0,55]). Az alacsony esetszám és heterogenitás miatt további vizsgálatok szükségesek.
Gonadotropinok mellé kiegészítő terápiaként alkalmazott MET szignifikánsan növeli a terhességek (OR: 2,25 [95% CI 1,50–3,38]) és az élveszületések esélyét (OR: 1,94 [95% CI: 1,10–3,44]) .
A metformin növeli az implantáció (beágyazódás) valószínűségét is (OR: 1,42 [95% CI: 1,24–2,75]), de nem javítja sem a terhesség, sem az élveszületések arányát. Ugyanakkor csökken a koraterhességi vesztesség (OR: 0,50 [95% CI: 0,30–0,83]) és az OHHS (hiperstimuláció) kialakulásának esélye (OR: 0,27 [95% CI: 0,16–0,46]).
Mind a gonadotropinokkal való kombinációban, mind IVF során alkalmazott MET eredményességének egyértelmű tisztázására további vizsgálatok szükségesek.
Kiegészítés
- A terhesség alatt alkalmazott MET terápia csökkenti a gesztációs diabetes (OR: 0,37 (CI: 0,25–0,56), a pre-eclampszia (OR: 0,53 [95% CI: 0,30–0,95]) és a koraszülés (OR: 0,30 (CI: 0,13–0,68) kockázatát.
- A kezelés során lényegesebb anyai mellékhatásokat nem észleltek és a lényegesebb magzati fejlődési rendellenességek száma sem emelkedett (OR: 0,86, [95% CI: 0,18–4,08])
- A kutatási eredmények ellenére Magyarországon a metformin terhesség alatt hivatalosan nem alkalmazható.
5. Inositol alkalmazásának lehetősége
10 randomizált kontrollált vizsgálatot (RTC) feldolgozó meta-analízis eredménye alapján az inozitol jelentősen javította az ovuláció esélyét (RR 2,3, 95% = 75%) és a menstruációs ciklus rendszerességét (RR 8,8, 95% CI 2,8, 16,6, I2 = 0%) a placebóval összehasonlítva.
Egy tanulmány számolt be az inozitol kedvező hatásáról klinikailag igazolt terhességi arányra vonatkozóan placebóval összehasonlítva (RR 3,3; 95% CI 0,4–27,1) és egy metforminnal történő összehasonlításról (RR 1,5; 95% CI 0,7–3,1). Ugyanakkor nincsenek tanulmányok az élveszületés és a vetélés arányának értékelése.
Kilenc randomizált vizsgálatot (RTC) feldolgozó meta-analízisben a MYO vagy a MYO + DCI hatását vizsgálták PCOS-ben kialakuló anyagcsere-rendellenességek kezelésére. Összesen 362 nő kapott inozitolt (
Hét tanulmány (összese 935 beteg) szisztematikus irodalmi áttekintése és az eredmények meta-analízise alapján, a myoinositol-kiegészítés szignifikánsan javította a klinikai terhességi arány IVF-ET [95% -os konfidencia intervallum (CI), 1,04–1,96; P = .03] és csökkentette az abortusz aránya (95% CI, 0,08–0,50; P =0,0006). Javult az embriók minőségét, és csökkentette a nem megfelelő minődégű petesejteket (oocyták) és ugyancsak csökkent az ovuláció indukció során felhasznál gyógyszer mennyisége.
6. Szelektív aromatáz inhibitorok alkalmazásának lehetősége
Antiösztrogén hatásuk miatt szelektív aromatáz inhibitorok alkalmazásának lehetősége is felmerül meddő PCOS betegek kezelésénél. Ugyanakkor az eddigi vizsgálatok szerint nem egyértelműek a letrozol és az anastrozol alkalmazásának előnyei a CC rezisztens esetekben, bár letrozol alkalmazása javította a születési arányt clomifen citráttal összehasonlítva (OR: 1,63 [95% CI: 1,31–2,03]).
A meddő PCOS betegek számára új lehetőség az aromatáz inhibítorok alkalmazása.
Az aromatáz inhibitorok (AI-k) a gyógyszerek azon csoportja, amelyeket 2001-ben vezettek be az ovuláció kiváltására. Körülbelül 2001 óta a klinikai vizsgálatok eltérő következtetésekre jutottak arra vonatkozóan, hogy az AI, a letrozol, legalább olyan hatékony-e, mint az első vonalbeli kezelés, a klomifén-citrát. CC), egy szelektív ösztrogén receptor modulátor (SERM).
Az AI-k leszabályozzák az ösztrogéntermelést az aromatáz izoenzimeinek gátlásával. Gátolják az ösztrogén negatív visszacsatolást a hipotalamuszban, és erősebb gonadotropin-releasing hormon (GnRH) impulzusokat eredményeznek. A megnövekedett GnRH szint az agyalapi mirigyet több FSH termelésére serkenti, ami tüszők kialakulását idézi elő a petefészekben.
Mivel az AI-k nem érintik az ösztrogénreceptorokat, ellentétben a CC-vel, a központi visszacsatolási mechanizmus érintetlen marad, és ahogy a domináns tüsző nő és az ösztrogénszint emelkedik, a normális negatív visszacsatolás központilag történik. Ez az FSH elnyomásához vezet, és a kisebb méretű tüszők atresián (sorvadáson) mennek keresztül. Ezért, ha a központi mechanizmust érintetlenül hagyják, az AI-k csökkenthetik a többszörös ovuláció és az OHSS kockázatát a CC-hez képest. és nem fejtenek ki antiösztrogén hatást a méhnyálkahártyában, ami esetleg nehezíti a beágyazódást.
Metaanalízis bizonyítékot mutat arra, hogy a PCOS-ben szenvedő nőknél megnövekedett élveszületési arány a letrozol javára, összehasonlítva a CC-vel. Ez eltér egy korábbi áttekintéstől, amely nem észlelt eltérést.
Megjegyzés: Az aromatáz inhibitorok Magyarországon csak emlőrák kezelésében vannak törzskönyvezve, de a kutatások alapján off label formábal gyakran alkalmazzák.
ÖSSZEFOGLALÁS
- A metformin és az inositol készítmények - bár kedvezően befolyásolhatják a menstruációs ciklus és a peteérést, ÖNMAGUKBAN GYAKRAN NEM ELEGENDŐEK a panaszok kezelésére.
- Ezért nőgyógyász-endokrinológussal történő konzultáció szükséges a megfelelő, peteérésre direkt módon ható készítmények kiválasztása és alkalmazása érdekében.
- Elhízás esetén törekedni a fogyásra az anyagcsere állapot javítása és az oxidatív stressz csökkentése érdekében.
FIGYELEM!
- ÖNMAGÁBAN A TESTTÖMEG CSÖKKENÉSE IS KEDVEZŐ LEHET A MENSTRUÁCIÓS ZAVAROK ÉS A MEDDŐSÉG KEZELÉSÉRE!
- FOGYÁSSAL RENDEZŐDHET A MENZESZ, NAGYOBB ESÉLLYEL FORDUL ELŐ PETEÉRÉS!
- FOGYÁSSAL CSÖKKEN A TERHESSÉG ALATT KIALAKULÓ SZÖVŐDMÉNYEK KIALAKULÁSÁNAK KOCKÁZATA!
Jelen tájékoztató nem helyettesíti orvosával történő személyes konzultációt vagy az Ön által használt készítmény betegtájékoztatójának elolvasását!
►Lásd még:
Metformin alkalmazása inzulinrezisztenciában
Metformin – újabb adatok egy megbízható és hatékony „régi” vércukorcsökkentő készítményről
Inositol alkalmazásának lehetőségei
Metformin és inositol összehasonlítása
Anti-Müller-hormon: a petefészekrezerv vizsgálata és ennek klinikai jelentősége
Irodalom
- Costello, M. F., Misso, M. L., Wong, J., et al. The treatment of infertility in polycystic ovary syndrome: a brief update. Aust. N. Z. J. Obstet. Gynaecol., 2012, 52(4), 400–403.
- Parsanezhad, M. E., Alborzi, S., Motazedian, S., et al.: Use of dexamethasone and clomiphene citrate in the treatment of clomiphene citrate-resistant patients with polycystic ovary syndrome and normal dehydroepiandrosterone sulfate levels: a prospective, double-blind, placebo-controlled trial. Fertil. Steril., 2002, 78(5), 1001–1004.
- Balen, A. H.: Ovulation induction in the management of anovulatory polycystic ovary syndrome. Mol. Cell. Endocrinol., 2013, 373(1–2), 77–82.
- Christin-Maitre, S., Hugues, J. N.: A comparative randomized multicentric study comparing the step-up versus step-down protocol in polycystic ovary syndrome. Hum. Reprod., 2003, 18(8), 1626–1631.
- Nugent, D., Vandekerckhove, P., Hughes, E., et al.: Gonadotrophin therapy for ovulation induction in subfertility associated with polycystic ovary syndrome. Cochrane Database Syst. Rev., 2000, 4, CD000410.
- Homburg, R., Hendriks, M. L., Konig, T. E., et al. Clomifene citrate or low-dose FSH for the first-line treatment of infertile women with anovulation associated with polycystic ovary syndrome: a prospective randomized multinational study. Hum. Reprod., 2012, 17(2), 468–473.
- Farquhar, C., Brown, J., Marjoribanks, J.: Laparoscopic drilling by diathermy or laser for ovulation induction in anovulatory polycystic ovary syndrome. Cochrane Database Syst. Rev., 2012, 6, CD001122.
- Xiao, J., Chen, S., Zhang, C., et al.: Effectiveness of GnRH antagonist in the treatment of patients with polycystic ovary syndrome undergoing IVF: a systematic review and meta analysis. Gynecol. Endocrinol., 2013, 29(3), 187–191.
- Misso, M. L., Wong, J. L., Teede, H. J., et al.: Aromatase inhibitors for PCOS: a systematic review and meta-analysis. J. Hum. Reprod. Update, 2012, 18(3), 301–312.
- Franik, S., Kremer J. A., Nelen, W. L., Farquhar, C.: Aromatase inhibitors for subfertile women with polycystic ovary syndrome. Cochrane Database Syst Rev. 2014, 2, CD010287.
- Lord, J. M., Flight, I. H., Norman, R. J.: Metformin in polycystic ovary syndrome: systematic review and meta-analysis BMJ, 2003, 327(7421), 951-953.
- Tang, T., Lord, J.M., Norman RJ, et al.: Insulin-sensitising drugs (metformin, rosiglitazone, pioglitazone, D-chiro-inositol) for women with polycystic ovary syndrome, oligo amenorrhoea and subfertility. Cochrane Database Syst. Rev., 2012, 5, CD003053.
- Palomba, S., Falbo, A., La Sala, G. B.: Metformin and gonadotropins for ovulation induction in patients with polycystic ovary syndrome: a systematic review with meta-analysis of randomized controlled trials. Reprod. Biol. Endocrinol., 2014, 12, 3.
- Palomba, S., Falbo, A., La Sala, G. B.: Effects of metformin in women with polycystic ovary syndrome treated with gonadotrophins for in vitro fertilisation and intracytoplasmic sperm injection cycles: a systematic review and meta-analysis of randomised controlled trials. BJOG, 2013, 120(3), 267-276.
- Pundir J. és mtsai: Inositol treatment of anovulation in women with polycystic ovary syndrome: a meta-analysis of randomised trials. BJOG. 2017 May 24. doi: 10.1111/1471-0528.14754. )
- Showell M.G. és mtsai: Inositol for subfertile women with polycystic ovary syndrome. Cochrane Database Syst Rev. 2018 Dec 20;12:CD012378. doi: 10.1002/14651858.CD012378.pub2.
- Unfer V. és mtsai: Effects of Inositol(s) in Women with PCOS: A Systematic Review of Randomized Controlled Trials. International Journal of Endocrinology 2016 (2016), Article ID 1849162, 12 pages)
- Unfer, V. és mtsai: Myo-inositol effects in women with PCOS: a meta-analysis of randomized controlled trials. Endocr Connect. 2017 Nov; 6(8): 647–658.
- Wang, R.és mtasi: Prognositic Value of CD73-Adenosinergic Pathway in Solid Tumor: A Meta-Analysis and Systematic Review. Oncotarget 2017, 8, 57327–57336.
- Sebastian Franik and al: Aromatase inhibitors (letrozole) for ovulation induction in infertile women with polycystic ovary syndrome Cochrane Database Syst Rev. 2022 Sep 27;2022(9):CD010287. doi: 10.1002/14651858.CD010287.pub4
Szeretne megoldást találni nőgyógyászati és endokrinológia panaszaival kapcsolatban? Szeretne javítani hormonegyensúlyán és egészségén?
Az alábbi problémákra nálam megnyugtató szakértői segítséget kap!
Nőgyógyászati panaszok • PCOS • Inzulinrezisztencia • Fokozott szőrnövekedés, pattanások • Elhízás • Meddőség • Pajzsmirigy- és mellékvese rendellenességek • Egyéb hormonális problémák.
Kattintson az alábbi lehetőségek egyikére.

.jpg)

.jpg)


.jpg)